Hər növ tələbə işini həyata keçiririk
tezisDshron turşuları.13. Fəsil səh.tədqiqat üsulları.32. Eksperimental hissə. Səhifə Fəsil sh. texnika və təcrübə üsulu. 40. Tədqiqatın nəticələri dörd fəsildə təqdim olunur. İlk iki fəsil (ədəbiyyat icmalı) işdə istifadə olunan analoq komplekslərə və tədqiqat metodlarına həsr edilmişdir. Eksperimental hissənin iki fəsli kompleksləşdirici maddələrin sintezi və tədqiqi haqqında məlumatlardan ibarətdir...
Nadir torpaq və digər elementlərin bəzi komplekslər, diaminosikloheksan və dikarbon turşularının izomerlərinin törəmələri ilə kompleksləşməsinin tədqiqi. (referat, kurs işi, diplom, nəzarət)
ƏDƏBİYYAT İCARƏSİ
I FƏSİL
DŞRBON TURŞUSU.13
1.1. Komplekslərin sintezi.-. 13
1.2. Turşu dissosiasiya sabitləri. on dörd,
1.3. SHM və maqnezium kompleksləri. . . 16
1.4. Komplekslər d - keçid və bəzi başqa elementlər.. 19
1.5. REE kompleksləri.23
FƏSİL P. TƏDQİQAT METODLARI.32
2.1. pH-metrik titrləmə üsulu. 32
2.1.1. Tetrabaz turşularının turşu dissosiasiya sabitlərinin təyini.. J32
2.1.2. Komplekslərin sabitlik sabitlərinin təyini üçün potensiometrik üsul. 33
2.2. Stasionar civə elektrodundan istifadə etməklə dolayı potensiometrik üsul.-.34
2.3. Damlayan mis amalgam elektroddan istifadə edərək dolayı potensiometrik üsul. 36
2.4. Spektroqrafik üsul. 38
EKSPERİMENTAL HİSSƏ
III FƏSİL TƏCRÜBƏ TEXNİKASI VƏ ÜSUL. 40
3.1. KPDK-DCG-nin sintezi.40
3.1.1. Trans-1,2-diaminosiklo-heksan-N N-dimalon turşusunun sintezi.. 41
3.1.2. Cis-1,3-diaminosikloheksan-N, N"-dimalon turşusunun sintezi.42
3.1.3. Trans-I, 4-diaminosikloheksan-N, N-dimalon turşusunun sintezi. . 43
3.1.4. Cis-1,4-diaminosikloheksan-N, N-dimalon turşusunun sintezi. . . 43
3.1.5. Trans-I,2-diaminosikloheksan-N, N"-disuksin turşusunun sintezi.44
3.1.6. KPDK-DCG-nin fiziki xassələri. 45
3.2. Başlanğıc materialları və istifadə olunan cihazlar. 46
3.3. Eksperimental nəticələrin riyazi emalı.. 47
Tədqiqatın nəticələri dörd fəsildə təqdim olunur. İlk iki fəsil (ədəbiyyat icmalı) işdə istifadə olunan analoq komplekslərə və tədqiqat metodlarına həsr edilmişdir. Eksperimental hissənin iki fəslində yeni komplekslərin kompleksləşmə qabiliyyətinin sintezi və öyrənilməsi haqqında məlumatlar var.
ƏDƏBİYYAT İCARƏSİ
G L, A B, A I.
DSHINOCYCLO İZOMERLƏRİNİN KOMPLEKSONLARI, TÖRƏMƏLƏRİ HAQQINDA
HEKSAN VƏ KOMPLEKSONLAR, DİKARBOXUN TƏRƏMƏLƏRİ
Digər işlər
tezis
Bu işin məqsədi bərk cismin mikroteksturasının əmələ gəlməsinə nəzarət etmək yollarını tapmaq üçün zəruri olan kalsium sulfat hemihidrat kristallarının böyüməsinin və aqreqasiyasının ayrı-ayrı mərhələlərini öyrənmək, həmçinin cismin fiziki və riyazi modelini yaratmaqdır. kristallaşma prosesi, onsuz optimal texnoloji prosesləri yaratmaq mümkün deyil. Bu işdə biz bir kompleksdən istifadə etdik...
tezis
Tədqiqatın nəticələrinə əsasən, sulfat məhlullarından REE-nin çıxarılması və ayrılması üçün yeni ekstraksiya üsulları hazırlanmışdır. Mövcud və geniş istifadə olunan reagentlərin qarışıqları - alkilfosfor turşuları və ilkin aminlər ekstraktorlar kimi tövsiyə olunur. Hazırlanmış üsullar kükürd turşusu ilə əldə edilən texnoloji məhlullardan nadir torpaq elementlərinin çıxarılması üçün genişmiqyaslı laboratoriya sınaqlarında yoxlanılıb...
tezis
1:2 Pd (AlaXAla")Cl və Pd (Ser)(Ser")Cl tərkibli alanin və serin ilə palladiumun (1D) komplekslərində bir amin turşusu molekulu palladiumla koordinasiyaya görə monodentat neytral liqanddır ( II) amin qrupunun azotunun. İkinci molekulun anionu amin qrupunun azotunun və karboksil qrupunun oksigeninin palladium (II) ilə koordinasiyasına görə bidenat siklik liqanddır. Kompleks birləşmələrdə...
tezis
Oksimlərin iki nümayəndəsi, salisialdoksim (aromatik benzoik sistem) və 1,2-naftoxinon-1-monoksim (aromatik quinoid sistem) liqandlar kimi istifadə edilmişdir. Əsas vəzifəyə əlavə olaraq - intrasferadakı liqandlar üçün elektrofilik reaksiyaların öyrənilməsi - əlavə vəzifələr qoyuldu: Alınan platin kompleksləri üçün elektron paylanmanın təbiətini və növünü təyin etmək ...
Elmi yenilik Müxtəlif təbiətli metallardan (Fe, Co, N1, Zn, Ce, Cc1, Pc1, Ag, Mo) və ya onların DND səthində lokallaşdırılmış qeyri-üzvi birləşmələrindən ibarət metal tərkibli nanohissəciklərin yaradılması imkanları tədqiq edilmişdir. Həcmində DND mikroqranullarının lokallaşdırıldığı, qeyri-üzvi nanohissəciklərlə bəzədilmiş LDPE matrisindən ibarət hibrid kompozit materiallar yaradılmışdır...
tezis
Elmi yenilik. Praktik dəyər. Silikon üzərində ferroelektrik xassələrə malik qurğuşun titanatının nazik təbəqəli strukturlarının məqsədyönlü sintezi üçün şərtlər işlənib hazırlanmışdır ki, bunlardan funksional elektronika qurğuları üçün istifadə oluna bilər. İşin aprobasiyası. İşin əsas nəticələri “Single Crystal Growth” Üçüncü Beynəlxalq Konfransının Materiallarında təqdim edilmiş və məruzə edilmişdir...
Hazırlanmış sintez üsulları müxtəlif trifloroasetat komplekslərinin alınması üçün istifadə edilə bilər. Trifloroasetat komplekslərinin sublimasiya proseslərinin və termoliz məhsullarının tədqiqi bu maddələrdən müxtəlif sahələrdə istifadə etməyə imkan verir. texnoloji proseslər. X-şüalarının difraksiya tədqiqatlarının nəticələri qeyri-üzvi və koordinasiya kimyasına əsaslı töhfə verir...
tezis
Tərkibində bir neçə metal ionu olan mürəkkəb tarazlıq sistemlərinin öyrənilməsində aktual istiqamət, onlardan biri paramaqnitdir, bu cür sistemlərin öyrənilməsi üçün ən etibarlı üsul proton maqnit relaksasiyası və riyazi modelləşdirmə üsullarının birləşməsidir. Bu metodlar toplusundan istifadə əsasən bu işin aktuallığını müəyyən edir" tədqiqatında...
Frolov Yu.V., Pivkina A.H. Heterojen sistemlərdə enerjinin ayrılması (yanma) proseslərinin fraktal quruluşu və xüsusiyyətləri // FGV. 1997. V. 33. No 5. S. 3−19. Tsunoda R., Ozawa T., Ando J. Kömür və qəhvə əsaslı aktiv karbonların ozon müalicəsi: su buxarının adsorbsiyası və səth fraktal mikroməsamələri // J. Coll. Int. elm. 1998. V. 205. S. 265−270. Rong H., Xuchang X., Changhe C., Hongli F...
tezis
Fiziki və fiziki Kimyəvi xassələri alkoqolatlar ümumiyyətlə iki əks tendensiyanın təsiri ilə müəyyən edilir - metalın alkoks qrupları ilə körpü bağları yaratmaqla koordinasiya sayını artırmaq istəyi və əks təsir - budaqlanmış alkil qrupları vəziyyətində yaranan sterik maneələr. Bu, geniş diapazonla nəticələnir...
tezis
İlk tikildi T-X mərhələsi Bu sistemlərin politermal bölmələrinin, mayeləşmə səthlərinin və izotermik kəsiklərinin diaqramları, şübhəsiz ki, yeni birləşmələrin sintezi üsullarının nəzəri və praktik inkişafı ilə əlaqədar tətbiq tapacaq və həmçinin istinad materialı kimi istifadə edilə bilər. Tetradimit quruluşlu birləşmələrin (Bi^Se^, Bi^Te^...) üstünlüklərinin termoelektrik fiquru haqqında
Müəlliflik hüququ ASC "Mərkəzi Dizayn Bürosu "BIBCOM" & MMC "Agency Kniga-Service" Əlyazması kimi Semenova Maria Gennadievna KOBALT(II) VƏ NİKEL(II) MONOAMİNLİKSİZLİKSİLİKSİLİKSİLİKSİLİKSİLİKSİLİKSİLİKSİLİKSİLİKSİLİKSİLİKSİLİKLƏRİNİN HOMO-LİQAND VƏ HETERO-LİQAND KOORDİNASİYA BİRLİKLƏRİ –0,020 qeyri-üzvi kimya Namizədlik elmi dərəcəsi almaq üçün dissertasiyanın REFERATI kimya elmləri Kazan – 2011 Müəlliflik hüququ ASC "Mərkəzi Dizayn Bürosu "BIBCOM" & MMC "Agentlik Kniga-Service" 2 İş "Udmurt Dövlət Universiteti" Ali Peşə Təhsili Dövlət Təhsil Müəssisəsində aparılmışdır. Rəhbər: kimya elmləri doktoru, professor Kornev Viktor İvanoviç Rəsmi opponentlər: kimya elmləri doktoru, professor Polovnyak Valentin Konstantinoviç kimya elmləri namizədi, professor Sentemov Valentin Vasilyeviç Aparıcı təşkilat: Kazan (Volqa bölgəsi) Dövlət Universiteti Müdafiə 31 may 2011-ci il saat 14:00-da dissertasiya şurasının iclasında keçiriləcək. D 212.080.03 Kazan Dövlət Texnologiya Universitetində 420015, Kazan, st. Karl Marks, ö. 68 (Elmi Şuranın konfrans zalı). Dissertasiya ilə burada tanış olmaq olar elmi kitabxana Kazan Dövlət Texnologiya Universiteti. Avtoreferat göndərildi “___” aprel 2011 Dissertasiya şurasının elmi katibi Tretyakova A.Ya. Müəlliflik hüququ SC "Mərkəzi Dizayn Bürosu "BIBCOM" & MMC "Agentlik Book-Servis" 3 İŞİN ÜMUMİ XÜSUSİYYƏTLƏRİ Mövzunun aktuallığı. Tarazlıq sistemlərində heteroliqand komplekslərinin əmələ gəlməsi qanunauyğunluqlarının öyrənilməsi innovativ kimyəvi texnologiyaların tətbiqi ilə ayrılmaz şəkildə əlaqəli olan koordinasiya kimyasının əsas problemlərindən biridir. Kobalt(II) və nikel(II)-nin sulu məhlullarda kompleksonlar və dikarbon turşuları ilə kompleks əmələ gəlməsinin tədqiqi əsaslandırma və modelləşdirmə üçün çox faydalıdır. kimyəvi proseslər polikomponent sistemlərdə. Bu liqandların sintetik mövcudluğu və modifikasiyasının geniş imkanları onların əsasında tələb olunan xassələrə malik kompleks əmələ gətirən kompozisiyalar yaratmaq üçün böyük potensial yaradır. Kobalt(II) və nikel(II)-nin tədqiq olunan liqandlarla koordinasiya birləşmələri haqqında ədəbiyyatda mövcud olan məlumatlar zəif sistemləşdirilmiş və bir sıra liqandlar üçün natamamdır. Heteroliqand kompleksi haqqında praktiki olaraq heç bir məlumat yoxdur. Nəzərə alınan reagentlərlə Co(II) və Ni(II) komplekslərinin kifayət qədər tədqiq edilmədiyini və alınan nəticələrin çox ziddiyyətli olduğunu nəzərə alaraq, bu sistemlərdə və eyni eksperimental şəraitdə ion tarazlığının tədqiqi aparılır. çox vacib. Yalnız bütün növ qarşılıqlı əlaqənin nəzərə alınması mürəkkəb çoxkomponentli sistemlərdə tarazlıq vəziyyətinin adekvat mənzərəsini verə bilər. Yuxarıdakı mülahizələrin işığında kobalt(II) və nikel(II) duzlarının kompleksonlar və dikarbon turşuları ilə kompleks əmələ gəlməsi proseslərinin məqsədyönlü və sistemli tədqiqatlarının koordinasiya kimyası üçün aktuallığı aşkar və əhəmiyyətli görünür. İş məqsədləri. Sulu məhlullarda monoaminkarboksimetil kompleksonları və doymuş dikarbon turşuları ilə kobalt(II) və nikel(II)-nin homo- və heteroliqand komplekslərinin əmələ gəlməsinin tarazlığının müəyyən edilməsi və xüsusiyyətlərinin müəyyən edilməsi. Qarşıya qoyulan məqsədə nail olmaq üçün qarşıya aşağıdakı vəzifələr qoyulmuşdur: tədqiq olunan liqandların turşu-qələvi xassələrinin, həmçinin kobalt(II) və nikel(II)-nin homo- və heteroliqand komplekslərinin əmələ gəlməsi şərtlərinin eksperimental şəkildə tədqiqi. geniş pH dəyərləri və reagentlərin konsentrasiyası; binar və üçlü sistemlərdə komplekslərin stoxiometriyasını təyin etmək; tədqiq olunan sistemlərdə reallaşdırılan bütün tarazlıqların tamlığı nəzərə alınmaqla mürəkkəb formalaşma proseslərinin riyazi modelləşdirilməsini həyata keçirmək; Müəlliflik hüququ ASC «Mərkəzi Dizayn Bürosu «BIBCOM» və MMC «Agency Kniga-Service» 4 komplekslərin mövcudluğu üçün pH dəyərlərinin diapazonunu və onların yığılma payını müəyyən etmək; aşkar edilmiş komplekslərin sabitlik sabitlərini hesablamaq; reaksiyaların mütənasibləşməsi sabitlərini təyin edin və metal kationlarının koordinasiya sferasında liqandların uyğunluğu haqqında nəticə çıxarın. Elmi yenilik. İlk dəfə olaraq monoamin karboksimetil xelatatorları ilə kobalt(II) və nikel(II)-nin homo- və heteroliqand komplekslərinin sistematik tədqiqi: iminodiasetik (IDA, H2Ida), 2-hidroksietiliminodiasetik (HEIDA, H2Heida), nitrilothiasetik (NTA) ), metilglisindioasetik (MGDA, H3Mgda) turşuları və məhdudlaşdırıcı seriyanın dikarboksilik turşuları: oksalik (H2Ox), malonik (H2Mal) və süksinik (H2Suc). Məhlullarda qarşılıqlı təsir öyrənilən sistemlərin çoxkomponentli təbiəti nöqteyi-nəzərindən nəzərdən keçirilir ki, bu da məhlulda müxtəlif rəqabətli reaksiyaların mövcudluğunu müəyyən edir. Tərkibində kobalt (II) və nikel (II) duzları, həmçinin monoamin kompleksləri və dikarbon turşuları olan sistemlərdə homojen tarazlığın kəmiyyət təsvirinin nəticələri yenidir. İlk dəfə olaraq heteroliqand komplekslərinin stoxiometriyası müəyyən edilmiş, tədqiq olunan liqandlarla reaksiyaların tarazlıq sabitləri və Co(II) və Ni(II) komplekslərinin dayanıqlıq sabitləri müəyyən edilmişdir. praktiki dəyər. Müxtəlif fiziki-kimyəvi tədqiq metodlarından istifadə etməklə kobalt(II) və nikel(II)-nin monoaminkarboksimetil kompleksonları və dikarboksilik turşuların məhdudlaşdırıcı sıra ilə kompleks əmələ gəlməsinin öyrənilməsinə əsaslandırılmış yanaşma təklif edilmişdir.Bunların homo- və heteroliqand komplekslərinin sabitlik sabitləri. metallar. Kobalt(II) və nikel(II) komplekslərinin stexiometriyası və termodinamik dayanıqlığı baxımından tədqiq olunan sistemlərin hərtərəfli təhlili xelatların quruluşu ilə onların kompleksləşmə xassələri arasında bəzi qanunauyğunluqları müəyyən etməyə imkan vermişdir. Bu məlumat kompleksonlara və dikarbon turşularına əsaslanan kompleksləşdirici kompozisiyalardan istifadə etməklə öyrənilən kationların təyini və maskalanması üçün kəmiyyət üsullarının işlənib hazırlanmasında faydalı ola bilər. Əldə edilən məlumatlar istənilən xüsusiyyətlərə və yaxşı performans xüsusiyyətlərinə malik texnoloji həllər yaratmaq üçün istifadə edilə bilər. Müəllif hüququ ASC "Mərkəzi Dizayn Bürosu" BIBCOM " & MMC "Agentlik Kniga-Service" 5 Reaksiya tarazlığı sabitlərinin tapılmış dəyərləri istinad kimi qəbul edilə bilər. İşdə əldə edilən məlumatlar onların tədris prosesində istifadəsi üçün faydalıdır. Müdafiəyə təqdim edilən əsas müddəalar: öyrənilən liqandların turşu-qələvi xassələrinin, protolitik tarazlıqlarının və mövcudluq formalarının tədqiqinin nəticələri; müxtəlif rəqabətli qarşılıqlı təsirlər şəraitində monoamin karboksimetil kompleksonları və dikarbon turşuları ilə kobalt(II) və nikel(II)-nin homo- və heteroliqand komplekslərinin əmələ gəlməsinin qanunauyğunluqları; spektrofotometriya və potensiometriya məlumatlarına əsasən mürəkkəb polikomponent sistemlərdə tarazlığın riyazi modelləşdirilməsinin nəticələri; tədqiq olunan sistemlərdə kompleks formalaşma proseslərinə müxtəlif amillərin təsiri; komplekslərin stoxiometriyası, reaksiyaların tarazlıq sabitləri, əmələ gələn komplekslərin koproporsional sabitlikləri və sabitlik sabitləri, onların əmələ gəlməsi və mövcudluğunun pH diapazonları, həmçinin liqand konsentrasiyalarının komplekslərin yığılma payına təsiri. Müəllifin şəxsi töhfəsi. Müəllif tədqiqatın əvvəlində problemin vəziyyətini təhlil etmiş, məqsədini formalaşdırmış, eksperimental iş aparmış, tədqiqat predmetinin nəzəri əsaslarının işlənib hazırlanmasında iştirak etmiş, nəticələri müzakirə edərək nəşrə təqdim etmişdir. Görülən iş üzrə əsas nəticələr dissertant tərəfindən tərtib edilir. İşin aprobasiyası. Dissertasiya işinin əsas nəticələri Koordinasiya birləşmələri üzrə XXIV Beynəlxalq Çuqayev konfransında (Sankt-Peterburq, 2009), “Kimyəvi analiz” Ümumrusiya konfransında (Moskva – Klyazma, 2008), IX Rusiya Universitetinin Akademik Elmi və İ. Praktiki Konfrans (İjevsk, 2008), həmçinin Udmurt Dövlət Universitetinin illik yekun konfranslarında. Nəşrlər. Dissertasiya işinin materialları 14 nəşrdə, o cümlədən Ümumrusiya və Beynəlxalq elmi konfranslarda məruzələrin 6 tezisi və 8 məqalədə təqdim edilmişdir, bunlardan 5-i aparıcı resenziyalı elmi jurnallar və tövsiyə olunan nəşrlər siyahısına daxil edilmiş jurnallarda dərc edilmişdir. Rusiya Təhsil və Elm Nazirliyinin Ali Attestasiya Komissiyası tərəfindən. Müəlliflik hüququ ASC "Mərkəzi Konstruktor Bürosu" BIBCOM " & MMC "Agentlik Kitab-Servis" 6 Dissertasiyanın strukturu və həcmi. dissertasiya giriş, ədəbiyyat icmalı, eksperimental hissə, nəticələrin müzakirəsi, nəticələr və istinadlar siyahısından ibarətdir. Əsərin materialı 47 rəqəm və 13 cədvəl olmaqla 168 səhifədə təqdim edilmişdir. İstinad edilən ədəbiyyat siyahısında yerli və xarici müəlliflərin 208 adda əsəri var. İŞİN ƏSAS MƏZMUNU Kompleks əmələ gəlmə proseslərinin tədqiqi spektrofotometrik və potensiometrik üsullarla aparılmışdır. Məhlulların optik sıxlığı SF-26 və SF-56 spektrofotometrlərində kvars şüşələri və qalınlığı 5 sm qalınlığında uducu təbəqə ilə xüsusi hazırlanmış Teflon hüceyrədən istifadə etməklə ölçüldü.Belə bir hüceyrə eyni vaxtda pH dəyərini və optik sıxlığı ölçməyə imkan verir. həll. Bütün əyrilər A = f(pH) spektrofotometrik titrləmə yolu ilə əldə edilmişdir. Nəticələrin riyazi emalı CPESSP proqramı vasitəsilə həyata keçirilmişdir. Binar və üçlü sistemlərdə kompleksləşmənin tədqiqi kompleksonların və dikarbon turşularının iştirakı ilə Co(II) və Ni(II) perxlorat məhlullarının udma spektrlərinin formasının və optik sıxlığının dəyişməsinə əsaslanırdı. Bundan əlavə, biz heteroliqand kompleksləşməni nəzərə almadan üçlü sistemlər üçün kompleksləşmənin nəzəri modellərini qurmuşuq. A = f(pH) nəzəri asılılıqlarının təcrübə ilə müqayisəsi zamanı heteroliqand komplekslərinin əmələ gəlməsi prosesləri ilə bağlı kənarlaşmalar aşkar edilmişdir. İşçi dalğa uzunluqları kimi Co(II) birləşmələri üçün 500 və 520 nm, Ni(II) üçün 400 və 590 nm dalğa uzunluqları seçilmişdir ki, bu zaman müxtəlif pH dəyərlərində ligandların daxili udulması əhəmiyyətsizdir və kompleks birləşmələr əhəmiyyətli dərəcədə təsir göstərir. hiperkromik təsir. Tarazlıqları müəyyən edərkən metalların hər biri üçün monomer hidrolizin üç sabiti nəzərə alınmışdır. İşdə istifadə olunan kompleksonların və dikarboksilik turşuların dissosiasiya sabitləri Cədvəl 1-də verilmişdir. Monoamin karboksimetil kompleksonları iminodiasetik turşunun törəmələri kimi təqdim edilə bilər. ümumi formula H R + N CH2COO– CH2COOH burada R: –H (IDA), –CH2CH2OH (HEIDA), –CH2COOH –CH(CH3)COOH (MGDA). (NTA) və Müəllif Hüquqları ASC Mərkəzi Dizayn Bürosu BIBCOM & OOO Agency Kniga-Service 7 İşdə istifadə olunan məhdudlaşdırıcı seriyanın dikarboksilik turşuları ümumi Cn H2n(COOH)2 (H2Dik) düsturu ilə təmsil oluna bilər. M(II)–H2Dik sistemləri üçün A = f(pH) asılılığının xarakteri göstərdi ki, bir qayda olaraq, M(II)– istisna olmaqla, bu sistemlərin hər birində üç +, , 2– kompleksi əmələ gəlir. Bisdikarboksilatların əmələ gəlmədiyi H2Suc sistemi. Co(II)–H2Ox sistemində tarazlığın xarakterini müəyyən edə bilmədik, çünki bütün pH dəyərlərində kobalt(II) oksalatlarının az həll olunan çöküntüləri çökür və bu, məhlulun fotometrini qeyri-mümkün edir. Cədvəl 1. Komplekslərin və dikarbon turşularının I = 0,1 (NaClO4) və T = 20±2°С-də protonlaşma və dissosiasiya sabitləri 9,34 1,60 2,20 8,73 1,25 1,95 3,05 10,2 1,934.5 .1914.5 .1940. Məhlulların pH-nin artması deprotonasiyaya və orta metal dikarboksilatların əmələ gəlməsinə səbəb olur. Kompleks 3.0 regionunda formalaşmışdır< рН < 8.0 и уже при соотношении 1: 1 имеет долю накопления 73%. Содержание комплекса 2– равно 14, 88 и 100% для 1: 1, 1: 2 и 1: 5 соответственно в области 3.0 < рН < 10.1. Аналогичные процессы протекают в системах M(II)–H2Mal. Увеличение концентрации малоновой кислоты сказывается на доле накопления комплекса , так для соотношения 1: 1 α = 60 % (6.3 < рН < 8.5), а для 1: 10 α = 72 % (2.0 < рН < 4.4). Содержание в растворе комплекса 2– возрастает c 64% до 91% для соотношений 1: 10 и 1: 50 (6.0 < рН 9.5). Максимальные доли накопления комплекса и 2– при оптимальных значениях рН составляют 70 и 80% для соотношения концентраций 1: 10 и 54 и 96% для 1: 50. Увеличение концентрации янтарной кислоты в системах M(II)–H2Suc способствует возрастанию долей накопления комплексов [МSuc] и [МHSuc]+ и смещению области их формирования в более кислую среду. Например, доли накопления комплекса при соотношении концентраций 1: 1, 1: 10 и 1: 40 соответственно равны 16, 68 и 90 %. Содержание комплексов Copyright ОАО «ЦКБ «БИБКОМ» & ООО «Aгентство Kнига-Cервис» 8 + и при соотношении 1: 50 равно 54% (рНопт. = 3.9) и 97% (рНопт. = 7.7) соответственно. Константы устойчивости дикарбоксилатов Co(II) и Ni(II), рассчитанные методом последовательных итераций приведены в таблице 2. Полученные нами величины хорошо согласуются с рядом литературных источников. Математическая обработка кривых A = f(pH) и α = f(pH) проведенная путем последовательного рассмотрения моделей равновесий с участием Co(II) и Ni(II) и моноаминных комплексонов (HxComp) показала, что во всех исследованных двойных системах типа M(II)–HxComp образуется несколько комплексов. В качестве примера на рис. 1 представлены кривые A = f(pH) для систем Co(II)–H2Heida (а) и Ni(II)–H2Heida (б). А а А б 0.5 0.4 3 0.4 3 4 0.3 4 5 0.3 1 0.2 0.2 0.1 0 5 2 0.1 0 2 4 6 8 10 рН 0 2 4 6 8 10 рН Рис. 1. Зависимость оптической плотности растворов от рН для кобальта(II) (1) и никеля(II) (2) и их комплексов с H2 Heida при соотношении компонентов 1: 1 (3), 1: 2 (4), 1: 5 (5), ССо2+ = 6∙10–3, СNi2+ = 8∙10–3 моль/дм3, λ = 520 (а), 400 нм (б). Методами насыщения и изомолярных серий установлено мольное соотношение компонентов в комплексонатах в зависимости от кислотности среды равное 1: 1 и 1: 2. Мольный состав комплексов подтвержден также методом математического моделирования. При эквимолярном соотношении компонентов стопроцентная доля накопления наблюдается только для комплексов – и –, а для комплексов , , и значения αmax равны 82, 98, 85 и 99% соответственно. В слабокислой среде монокомплексонаты Co(II) и Ni(II) присоединяют второй анион комплексона, образуя средние бискомплексонаты 2(1–x). При двукратном избытке комплексона максимальные доли накопления комплексов 2–, 2– и Copyright ОАО «ЦКБ «БИБКОМ» & ООО «Aгентство Kнига-Cервис» 9 4– находятся в пределах 88 – 99% для области 8.6 < рН < 11.6. В данном интервале рН накапливаются и комплексы 4– и 4–, для которых αmax достигает 56 и 72% соответственно. Одновременно с бискомплексонатами металлов в двойных системах, за исключением систем M(II)–H2Ida в щелочной среде образуется также гидроксокомплексы 1–x. Константы устойчивости комплексонатов Co(II) и Ni(II) представлены в таблице 2. Таблица 2. Области значений рН существования и константы устойчивости дикарбоксилатов и комплексонатов кобальта(II) и никеля(II) при I = 0.1 и Т = 20 ± 2°С Комплекс Области рН существования lg Комплекс Области рН существования lg + 2– + 2– + 2– 2– – – 4– 2– – – – 0.4–5.5 >1.9> 3.6 2.0-12.0> 4.6 1.4-12.0> 4.8.8> 5.1.) 4.75 ± 0.98 ± 0.06 2.97 ± 0.08 6.0.29 ± 0.09 1.18 ± 0.09 1.18 ± 0.09 1.18 ± 0.09 11.69 ± 0,09 11.69 ± 0.16 8,16 ± 0,14 12,28 ± 0,66 11,88 ± 0,37 10,10 ± 0,76 13,50 ± 0,12 12,50 ± 0,09 + 2– + 2– + 2– 2– – 2– + 2– 2– – .2 >1–3 >1–3 >1–3 >1–3. 2.8 1.2-5.9> 2.1 1.0-12.0> 0.8> 4.3> 9.3.30 ± 0.30 ± 0.30.30 ± 0.07 5.30 ± 0.07 6.39.30.39.30.39.30.39.39.39.39.39.3. 0.05 14.20 ± 0.06 12.05 ± 0.11 ± 0.05 ± 0.05 ± 0.05 ± 0.76 16.34 ± 0.05 13.95 ± 0.09 - 4- 2- 2- 2- 2.1> 7.0> 7.0> 7.0.0.0.0.0.0.0.0.0:0.0. 0,24 15.29 ± 0,24 15.27 ± 0,58 11.27 ± 0,58 11.27 ± 0,58 11.27 4– 13,08 ± 0,72 2– *Ədəbiyyat məlumatları Üçlü sistemlərdə kompleksləşmə prosesləri həm də reagentlərin konsentrasiyasından və mühitin turşuluğundan asılıdır. Heteroliqand komplekslərinin əmələ gəlməsi üçün liqandların hər birinin konsentrasiyası homoliqand kompleksinin maksimum yığılması ilə binar sistemlərdə onların konsentrasiyasından az olmamalıdır. Müəlliflik hüququ ASC "Mərkəzi Dizayn Bürosu "BIBCOM" & MMC "Agency Kniga-Service" 10 Müəyyən edilmişdir ki, bütün üçlü sistemlərdə heteroliqand kompleksləri 1: 1: 1 və 1: 2: 1 molyar nisbəti ilə əmələ gəlir. yalnız 1:1:1 komplekslərinin əmələ gəldiyi M(II)–H2Ida sistemləri üçün –H2Dik.Heteroliqand komplekslərin mövcudluğunun sübutu nəzəri əyrilərin A = f(pH) nəzərə alınmadan hesablanması idi. heteroliqand kompleksinin formalaşması eksperimental əyrilərdən nəzərəçarpacaq dərəcədə fərqlənir (Şəkil 2.) A 0,3 . Şəkil 2. Nikel(II) (1) və onun H2Ida (2), H2Ox (3), H2Ida + H2Ox (4, 6) ilə kompleksləri üçün məhlulların optik sıxlığının pH-dan asılılığı, nəzərə alınmadan hesablanmış əyri. heteroliqand kompleksləri (5), komponentlərin nisbəti 1: 5 (2), 1: 2 (3), 1: 2: 2 (4, 5), 1: 2: 5 (6); СNi2+ = 8∙10–3 mol/dm3. 2 0,2 4 6 5 0,1 3 1 0 0 2 4 6 8 10 pH M(II)–H2Ida–H2Dik sistemlərində üç növ –, 2– və 3– komplekslərinin əmələ gəlməsi mümkündür. Üstəlik, sistemdə oksalat turşusu varsa, o zaman Co(II) və Ni(II) oksalatlar struktur hissəciklər kimi çıxış edir. H2Mal və ya H2Suc olan üçlü sistemlərdə ilkin liqandın rolunu bu metalların iminodiasetatları oynayır. Protonlanmış komplekslər yalnız М(II)–H2Ida–H2Ox sistemlərində əmələ gəlir. Komplekslər – və – güclü turşu mühitində və 2,5 diapazonunda əmələ gəlir< рН < 3.0 их содержание достигает 21 и 51% соответственно (для соотношения 1: 2: 2). В слабокислой среде кислые комплексы депротонируются с образованием средних гетеролигандных комплексов состава 2– и 2–, максимальные доли накопления которых при рН = 6.5 – 6.6 соответствеено равны 96 и 85% (для 1: 2: 2). При рН > 10.0 kompleks 2– hidroliz edilir və 3– əmələ gəlir. Oxşar proseslər M(II)–H2Ida–H2Mal sistemlərində baş verir. 2- və 2- komplekslərinin maksimum yığılma fraksiyaları 80 və 64% təşkil edir (1:2:10 və pH = 6,4 üçün). Qələvi mühitdə mühit kompleksləri 3- tipli hidroksokomplekslərə çevrilir. Müəllif Hüquqları ASC Mərkəzi Dizayn Bürosu BIBCOM & LLC Agency Kniga-Service 11 M(II) – H2Ida – H2Suc sistemlərindəki tarazlıq hətta H2Suc-un böyük həddən artıq həddindən artıq olduqda belə Co(II) və Ni(II) iminodiasetatlara doğru kəskin şəkildə dəyişir. Beləliklə, 1 : 2 : 50 nisbətində bu sistemlərdə yalnız 2- və 2- tərkibli orta komplekslər əmələ gəlir, məhluldakı tərkibi müvafiq olaraq 60 və 53% təşkil edir (рН = 6.4). M(II)–H2Heida–H2Dik sistemlərində dörd növ kompleksin əmələ gəlməsi mümkündür: –, 2–, 4– və 3– . Protonlanmış heteroliqand kompleksi həm tədqiq olunan metallar, həm də – kompleksindən başqa bütün liqandlar üçün tapıldı. Orta komplekslər 2- və 4- zəif turşulu və qələvi mühitlərdə pH = 5,8 və 9,5 (1:2:1 üçün) uyğun olaraq maksimum yığılma payı 72 və 68% olan mühitlərdə əmələ gəlir. HEIDA məhlulunda olan nikel(II) oksalatlar –, 2– və 4– tərkibləri ilə heteroliqand kompleksləri əmələ gətirir; M(II)–H2 Heida–H2Mal sistemində heteroliqand komplekslərinin əmələ gəlməsinin tamlığı H2Mal konsentrasiyasından çox asılıdır. Məsələn, Ni(II)–H2Heida–H2Mal sistemində 1 : 2 : 10 konsentrasiya nisbətində –, 2– və 4– komplekslərinin maksimum yığılma fraksiyaları pH 4.0 üçün 46, 65 və 11% təşkil edir. , müvafiq olaraq 6.0 və 10.5. Malon turşusunun konsentrasiyasının 50 dəfə artması ilə bu komplekslərin eyni pH dəyərlərində yığılma nisbətləri müvafiq olaraq 76, 84 və 31% -ə qədər artır. 1:2:75 komponent nisbətində Co(II)–H2 Heida–H2Mal sistemində aşağıdakı çevrilmələr baş verir: – αmax = 85%, pH = 3.4 – H+ 2– αmax = 96%, pH = 6.5 + Heida2– 4– αmax = 52%, pH = 9.8 M(II)–H2 Heida–H2Suc sistemlərində heteroliqand kompleksləri yalnız süksin turşusunun böyük miqdarda artıqlığında əmələ gəlir. Beləliklə, 1: 2: 100 nisbətində –, 2– və 4– komplekslərinin maksimum yığılma fraksiyaları 67 (рН = 4.8), 78 (рН = 6.4) və 75% (рН = 9.0) təşkil edir. və komplekslər üçün müvafiq olaraq –, 2– və 4– – 4 (рН = 4,6), 39 (рН = 6,0) və 6% (рН = 9,0–13,0). Oxşar proseslər M(II)–H3Nta–H2Dik sistemlərində baş verir. Turşu mühitdə oksalat turşusu olduqda, az miqdarda 2- kompleksi olan məhlulda Co(II) və Ni(II) oksalatlar üstünlük təşkil edir. Neytral mühitə yaxın orta heteroliqan kompleksləri 3- və 3- pH = 6 üçün maksimum yığılma hissəsi 78 və 12 90% ilə formalaşır. müvafiq olaraq 9 və 6.4. NTA artıqlığı olan qələvi mühitdə reaksiya 4- və 6- komplekslərinin əmələ gəlməsi ilə iki istiqamətdə gedir. Sonuncular böyük miqdarda toplanır, məsələn, 6- kompleksinin yığılma payı pH = 7.0 olduqda 82% -ə çatır. Co(II)–H3Nta–H2Mal sistemində komplekslərin fraksiya paylanması Şəkildə göstərilmişdir. 3. α, % d c a 80 b d b 60 b c c a 40 b d a c d d c d b c 20 a b aa 0 + pH = 2.3 – pH = 3.2 2– pH = 3.8 2– pH = 6.8 4– pH = 10.5 6– pH = 10.5. Şəkil 3. Müxtəlif pH dəyərlərində və komponentlərin müxtəlif nisbətlərində komplekslərin yığılma nisbətləri: 1:2:5 (a), 1:2:20 (b), 1:2:40 (c), 1: 2:80 (d) c Co(II)–H3Nta–H2Mal sistemi. M(II)–H3Nta–H2Suc sistemlərində struktur liqand H3Nta-dır və süksinik turşu əlavə liqand rolunu oynayır. H2Suc konsentrasiyasının artması heteroliqand komplekslərinin yığılma nisbətinin artmasına səbəb olur. Beləliklə, süksin turşusunun tərkibində 0,0-dan 0,12 mol/dm3-ə qədər artım kompleks 3-ün α dəyərinin 47-dən 76%-ə, protonlaşdırılmış kompleks 2-nin tərkibi isə 34-dən 63%-ə qədər artmasına səbəb olur ( pH = 4.3-də). Təxminən eyni nisbətdə 3- və 2- komplekslərinin pay nisbəti dəyişir. Qələvi mühitdə 3- kompleksləri başqa bir H3Nta molekulu ilə birləşir və 6- tərkibli komplekslər əmələ gəlir. 6- kompleksinin maksimum yığılması 1:2:40 nisbəti üçün pH = 10,3-də 43%, müvafiq nikel(II) kompleksi üçün, pH = 10,0-da α = 44%, 1:2 nisbətində: 50. heteroliqand kompleksləri 4- tərkibli hidroksokomplekslərin əmələ gəlməsi ilə hidroliz edilir. Müəlliflik hüququ ASC "Mərkəzi Dizayn Bürosu "BIBCOM" & OOO "Agency Kniga-Service" 13 M(II)–H3Nta–H2Suc sistemlərində homoliqand kompleksləri yalnız mövcuddur – və 4–, suksinat kompleksləri aşkar edilmir. Cədvəl 3. I = 0,1 (NaClO4) və T = 20±2°С Kompleks H2Ox H2Mal H2Suc – 2– 3– – 2– üçün kobalt(II) və nikel(II) kompleksonları və dikarbon turşuları ilə heteroliqand komplekslərinin sabitlik sabitləri. 3– – 2– 4– 3– – 2– 4– 3– 2– 3– 6– 4– 2– 3– 6– 4– 2– 3– 4– 2– 3– 6 - 4- 14.90 ± 0.19 11.27 0.66 - 17.38 ± 0.01 0. 0.01 ± 0.01 ± 0.61 ± 0.01 0. 0.01 0. 0.39 ± 0.0.39 ± 0.39 ± 0.39 ± 0.39 ± 0.39 ± 0.39 ± 0.39 ± 0.31 12.0.39 - 14.9.6.6.39. 0,24 18,98 ± 0,05 17,70 ± 0,09 16,99 ± 0,26 13,36 ± 0,73 15,73 ± 0,14 ± 0,25 ± 0,28 ± 0,19 - - 9,01 ± 0,20. - 7,01. 76 ± 0.38 - 15,58 ± 0,28 11.07 ± 0.43 14.07 ± 1.09 14.18 ± 0.52 16.15 ± 0.19 ± 1.30 12,17 ± 0,68 ± 1,30 12,17 ± 0,68 ± 0,17 ± 0,34 ± 0,04 14,95 ± 0,09 16,93 ± 0,46 ± 0,10 ± 0,45 17.50 ± 0.16 15.85 ± 0.09 16.93.93.93.93 0.93 15.28 ± 0.71 15.28 ± 0.76 17.266 ± 0.72 16.65 ± 0.72 16.65 ± 0.67 - 9.66 - 9.67 - 9.66 ± 0.65 ± 1.65 ± 1.55 ± 0.79 ± 0.75 ± 0.79 ± 0.75 ± 0.79 ± 0.34 11.65 ± 0.17 15.05 ± 0.10 15.05 ± 0.03 17.79 ± 0.34 12.03 ± 0,34 12.03 ± 0,06 16.03 ± 0,06 16.03 ± 0,06 16.03 ± 0,34 ± 0,34 ± 0,95 - 16.83 ± 0.43 - Xidmət 14 M(II)–H3Mgda–H2Dik sistemlərində dörd növ kompleksin əmələ gəlməsi də mümkündür: 2–, 3–, 6– və 4–. Lakin bu komplekslərin heç də hamısı ayrı-ayrı sistemlərdə əmələ gəlmir. Hər iki metal oksalat turşusu məhlullarında protonlanmış komplekslər əmələ gətirir, Co(II) isə malon turşusu məhlullarında da əmələ gəlir. Bu komplekslərin yığılma payı böyük deyil və bir qayda olaraq, 10% -dən çox deyil. Yalnız kompleks 2– αmax = 21% pH = 4.0 və komponent nisbəti 1:2:50. Kompleks 3– tərkibi oksalik turşunun konsentrasiyasının artması ilə əhəmiyyətli dərəcədə artır. H2Ox-un ikiqat artıqlığı ilə bu kompleksin yığılma payı 6.0 bölgəsində 43% təşkil edir.< рН < 9.0, а при десятикратном она увеличивается до 80%. При рН >10.0, oksalat ionlarının yüksək konsentrasiyasında belə, bu kompleks 4- əmələ gətirmək üçün hidroliz edilir. Nikel(II) kompleksi 3– regionda əmələ gəlir 6.4< рН < 7.9 и для соотношения компонентов 1: 2: 10 доля его накопления составляет 96%. При рН >7.0, məhlulda 6- tərkibli başqa bir orta heteroliqand kompleksi əmələ gəlir (pH temperaturunda α = 67% = 11.3). H2Ox konsentrasiyasının daha da artması bu komplekslər üçün α-nın dəyərinə praktiki olaraq heç bir təsir göstərmir. 1:2:25 konsentrasiya nisbətində 3- və 6- komplekslərinin yığılma payları müvafiq olaraq 97 və 68% təşkil edir. M(II)–H3Mgda–H2Ox sistemlərindəki struktur hissəcik oksalik turşudur. Əncirdə. Şəkil 4-də M(II)–H3Mgda–H2Mal sistemlərində tarazlıq vəziyyətini xarakterizə edən α = f(pH) və А = f(pH) əyriləri göstərilir. M(II)-H3Mgda-H2Suc sistemlərində heteroliqand kompleksinin formalaşması da süksinik turşunun konsentrasiyasından çox asılıdır. H2Suc-un on qat artıqlığında bu sistemlərdə heteroliqand kompleksləri əmələ gəlmir. 6.5 aralığında 1: 2: 25 konsentrasiya nisbəti ilə< рН < 9.0 образуются комплексы 3– (αmax = 10%) и 3– (αmax = 8%)/ Пятидесятикратный избыток янтарной кислоты увеличивает содержание этих комплексов до 15 – 16%. При стократном избытке H2Suc области значений рН существования комплексов 3– значительно расширяются, а максимальная доля накопления их возрастает приблизительно до 28 – 30%. Следует отметить, что для образования гетеролигандного комплекса в растворе необходимо определенное геометрическое подобие структур реагирующих гомолигандных комплексов, причем структура свойственная гомолигандному комплексу стабилизируется в гетеролигандном. Copyright ОАО «ЦКБ «БИБКОМ» & ООО «Aгентство Kнига-Cервис» 15 α 1.0 а А 2 4 1 6 3 0 2 7 6 8 б 2 10 A 4 1 0.3 0.2 5 4 1.0 0.4 9 0.5 α 0.2 6 0.5 8 7 0.1 рН 0.1 3 0 2 4 6 8 10 рН Рис. 4. Зависимость долей накопления комплексов (α) и оптической плотности растворов (A) от рН в системах Co(II)–H3Mgda–H2Mal (а) и Ni(II)–H3Mgda–H2Mal (б) для соотношения 1: 2: 50: экспериментальная кривая A = f(pH) (1), М2+ (2), [МHMal]+ (3), – (4), 2– (5), 3– (6), 4– (7), 6– (8), 4– (9); СCo2+ = 3∙10–3, СNi2+ = 4∙10–3 моль/дм3. Одним из факторов, определяющих стехиометрию и устойчивость гетеролигандных комплексов является совместимость лиганда в координационной сфере катиона металла. Мерой совместимости служит константа сопропорционирования Kd, характеризующая равновесия вида: 2(1–x) + 4– 2 x– В случае Kd > Koordinasiya sferasında 1 (və ya lgKd > 0) liqandlar uyğun gəlir. Bizim heteroliqand komplekslərimiz üçün Kd qiyməti (Kd = β2111/βMComp2βMDik2) həmişə birlikdən böyükdür ki, bu da Co(II) və Ni(II) koordinasiya sferasında liqandların uyğunluğunu göstərir. Bundan əlavə, bütün hallarda, heteroliqand kompleksinin lgβ111 dəyəri müvafiq biskomplekslərin lgβ dəyərlərinin həndəsi ortasını üstələyir, bu da liqandların uyğunluğunu göstərir. NƏTİCƏLƏR 1. Suda monoamin karboksimetil kompleksonları (IDA, HEIDA, NTA, MGDA) və doymuş dikarbon turşuları (oksalik, malonik, suksinik məhlullar) ilə kobalt(II) və nikel(II)-nin homo- və heteroliqand komplekslərinin sistematik tədqiqi aparılmışdır. ilk dəfə həyata keçirilir. 24 üçlü sistemdə 14 ikili və 65 heteroliqand kompleksində 34 homoliqand kompleksi müəyyən edilmişdir. Müəlliflik hüququ ASC "Mərkəzi Dizayn Bürosu "BIBCOM" & MMC "Agency Kniga-Service" 16 2. Protolitik tarazlığın təbiətinə və komplekslərin formalaşmasının tamlığına müxtəlif amillərin təsiri müəyyən edilmişdir. Bütün homo- və heteroliqand kompleksləri üçün yığılma fraksiyaları mühitin turşuluğundan və reaksiya verən komponentlərin konsentrasiyasından asılı olaraq hesablanmışdır. Komplekslərin stoxiometriyası müxtəlif pH dəyərlərində, həmçinin liqandların müxtəlif konsentrasiyalarında mövcud olduqları bölgələrdə müəyyən edilmişdir. 3. Müəyyən edilmişdir ki, Co(II) və Ni(II) oksalatların və malonatların məhlullarında üç növ + və 2- kompleksləri, suksinatların məhlullarında isə yalnız iki + və tərkibli monokomplekslərə rast gəlinir. Dikarboksilatların yığılma payını artırmaq üçün dikarboksilik turşuların tərkibində dəfələrlə artım tələb olunur. Bu halda, bu komplekslərin mövcudluğunun təkcə stoxiometriya deyil, həm də pH diapazonları dəyişə bilər. 4. Göstərilmişdir ki, M(II) – HxComp sistemlərində komplekslərin stoxiometriyası mühitin turşuluğundan və liqandların konsentrasiyasından asılıdır. Turşu mühitlərdə, bütün sistemlərdə əvvəlcə 2–x kompleksləri əmələ gəlir ki, bunlar da bir qədər turşulu məhlullarda pH-ın artması ilə biskompleksonatlara 2(1–x) çevrilir. Komplekslərin 100% yığılması liqandın iki-üç dəfə artıq olmasını tələb edir, komplekslərin əmələ gəlməsi isə daha turşulu bölgəyə keçir. Komplekslərin meydana gəlməsinin tamlığı üçün - və - kompleksin artıqlığı tələb olunmur. Qələvi mühitdə kompleksonatlar 1-x əmələ gəlməsi ilə hidrolizə olunur. 5. M(II)–HxComp–H2Dik üçlü sistemlərində kompleks əmələgəlmə tarazlıqları ilk dəfə tədqiq edilmiş və 1–x, x–, 2x– və (1+x)– tərkibli heteroliqand kompleksləri aşkar edilmişdir. Müəyyən edilmişdir ki, bu komplekslərin yığılma fraksiyaları və onların çevrilmə ardıcıllığı mühitin turşuluğundan və dikarbon turşusunun konsentrasiyasından asılıdır. Metal kationlarının koordinasiya sferasında liqandların uyğunluğu koproporsiya sabitlərinin qiymətlərindən müəyyən edilmişdir. 6. Heteroliqand kompleksləşməsinin iki mexanizmi müəyyən edilmişdir. Onlardan birincisi dikarboksilat-kompleksonatdır ki, burada dikarboksilik turşu anionu ilkin struktur təyin edən liqand rolunu oynayır. Bu mexanizm M(II)–HxComp–H2Ox tipli bütün sistemlərdə, həmçinin bəzi M(II)–HxComp–H2Dik sistemlərində həyata keçirilir ki, burada HxComp H2Ida və H2 Heida, H2Dik isə H2Mal və H2Suc-dur. İkinci mexanizm kompleksonatodikarboksilatdır, burada struktur təyin edən liqand metal komplekson və ya kompleksonatdır. Bu mexanizm bütün M(II)–H3Comp–H2Dik sistemlərində özünü göstərir, burada H3Comp H3Nta və H3Mgda, H2Dik isə H2Mal və Hər iki mexanizm tədqiq olunan liqandların pH artması ilə heteroliqand kompleksinə bağlanma ardıcıllığını göstərir. 7. Homo- və heteroliqand komplekslərinin sabitlik sabitləri hesablanmış, optimal M(II) : H3Comp : H2Dik nisbətləri və kompleks hissəciklərin konsentrasiyalarının maksimum qiymətə çatdığı pH qiymətləri müəyyən edilmişdir. Müəyyən edilmişdir ki, homo- və heteroliqand komplekslərinin logβ qiymətləri silsilədə artır:< < , < < – < –, 2– ≈ 2– < 4– ≈ 4–, 2– < 2– < 3– < 3–, которые обусловлены строением, основностью и дентатностью хелатов, размерами хелатных циклов, а также величиной координационного числа металла и стерическими эффектами. Основные результаты диссертации опубликованы в ведущих журналах, рекомендованных ВАК: 1. 2. 3. 4. 5. Корнев В.И., Семенова М.Г., Меркулов Д.А. Однороднолигандные и смешанолигандные комплексы кобальта(II) и никеля(II) с нитрилотриуксусной кислотой и дикарбоновыми кислотами // Коорд. химия. – 2009. – Т. 35, № 7. – С. 527-534. Корнев В.И., Семенова М.Г. Физико-химические исследования равновесий в системах ион металла – органический лиганд. Часть 1. Взаимодействие кобальта(II) с 2-гидроксиэтилиминодиацетатом в водных растворах дикарбоновых кислот // Бутлеровские сообщения. – 2009. – Т.17, №5. – С.54-60. Семенова М.Г., Корнев В.И. Комплексонаты кобальта(II) и никеля(II) в водных растворах щавелевой кислоты // Химическая физика и мезоскопия. – 2010. – Т. 12, № 1. – С. 131-138. Корнев В.И., Семенова М.Г., Меркулов Д.А. Гетеролигандные комплексы кобальта(II) и никеля(II) с иминодиуксусной и дикарбоновыми кислотами в водном растворе // Коорд. химия. – 2010. – Т. 36, № 8. – С. 595-600. Семенова М.Г., Корнев В.И., Меркулов Д.А. Метилглициндиацетаты некоторых переходных металлов в водном растворе // Химическая физика и мезоскопия – 2010. – Т.12, № 3. – С.390-394. Copyright ОАО «ЦКБ «БИБКОМ» & ООО «Aгентство Kнига-Cервис» 18 в других изданиях: 6. 7. 8. 9. 10. 11. 12. 13. 14. Корнев В.И., Семенова М.Г. Гетеролигандные комплексы кобальта(II) с нитрилотриуксусной кислотой и дикарбоновыми кислотами // Вестник Удм. Университета. Физика. Химия – 2008. – № 2. – С. 65-72. Семенова М.Г., Корнев В.И, Меркулов Д.А. Исследование равновесий в водных растворах дикарбоксилатов кобальта(II) и никеля(II) // Всероссийская конференция «Химический анализ» – Тез. докл. – Москва-Клязьма, 2008 – С. 93-94. Корнев В.И., Семенова М.Г., Меркулов Д.А. Взаимодействие никеля(II) с нитрилотриуксусной кислотой в присутствии дикарбоновых кислот // Девятая Российская университетско-академическая научно-практическая конференция: Материалы конференции – Ижевск, 2008 – С. 103-105. Семенова М.Г., Корнев В.И. Смешанолигандное комплексообразование кобальта(II) с нитрилотриуксусной кислотой и дикарбоксилатами // Девятая Российская университетско-академическая научно-практическая конференция: Материалы конференции – Ижевск, 2008 – С. 107-109. Семенова М.Г., Корнев В.И. Гетеролигандные комплексы 2гидроксиэтилиминодиацетата кобальта(II) и дикарбоновых кислот // XXIV Международная Чугаевская конференция по координационной химии и Молодежная конференция-школа «Физико-химические методы в химии координационных соединений» – Санкт-Петербург, 2009. – С. 434-435. Корнев В.И., Семенова М.Г., Меркулов Д.А. Метилглициндиацетатные комплексы некоторых переходных металлов в водно-дикарбоксилатных растворах // Десятая Российская университетско-академическая научнопрактическая конференция: Материалы конференции – Ижевск, 2010 – С. 101-102. Корнев В.И., Семенова М.Г. Взаимодействие кобальта(II) и никеля(II) c комплексонами ряда карбоксиметиленаминов и малоновой кислотой в водном растворе // Вестник Удм. Университета. Физика. Химия. – 2010. – № 1. – С. 34-41. Корнев В.И., Семенова М.Г. Кислотно-основные и комплексообразующие свойства метилглициндиуксусной кислоты // Десятая Российская университетско-академическая научно-практическая конференция: Материалы конференции – Ижевск, 2010 – С. 104-105. Семенова М.Г., Корнев В.И. Метилглицинатные комплексы кобальта (II) и никеля(II) в водно-дикарбоксилатных растворах // Вестник Удм. Университета. Физика. Химия – 2010 – № 2. – С. 66-71.
1Kompleksonlar (poliaminopolikarboksilik turşular) ən çox istifadə edilən polidentat liqandlar sırasındadır. Son illərdə kompleksonlara, dikarboksilik turşuların törəmələrinə, xüsusən süksin turşusunun törəmələrinə maraq artmışdır ki, bu da onların sintezi üçün sadə və əlverişli üsulların inkişafı və bir sıra spesifik praktiki vasitələrin olması ilə əlaqədardır. faydalı xassələri.
CPNA-nın sintezi üçün ən vacib üsul malein turşusunun əsas və ya ikincil amin qrupu olan müxtəlif birləşmələrlə qarşılıqlı təsirinə əsaslanır. Belə birləşmələr kimi alifatik monoaminomonokarboksilik turşular götürülərsə, qarışıq tipli kompleksonlar (KST) alınır və malein turşusu ammonyakla qarşılıqlı təsirə girdikdə KPYAK-ın ən sadə nümayəndəsi olan iminodisuksin turşusu (İDYA) alınır. Sintezlər mülayim şəraitdə baş verir, yüksək temperatur və təzyiq tələb etmir və kifayət qədər yüksək məhsuldarlıqla xarakterizə olunur.
KPJK-nın praktik tətbiqindən danışarkən aşağıdakı sahələri ayırmaq olar.
1. Tikinti materiallarının istehsalı. Bu sahədə CNC-nin istifadəsi bağlayıcıların (sement, beton, gips və s.) Nəmləndirilməsi prosesini yavaşlatmaq qabiliyyətinə əsaslanır. Bu xüsusiyyət özlüyündə vacibdir, çünki bağlayıcıların bərkidilmə sürətini idarə etməyə imkan verir və hüceyrəli beton istehsalında da əhəmiyyətli miqdarda sementə qənaət etməyə imkan verir. Bu baxımdan ən təsirli olanlar IDYAK və KST.
2. Yumşaq lehimləmə üçün suda həll olunan axınlar. Bu cür axınlar xüsusilə elektrik və radiotexnika sənayesi üçün aktualdır, burada çap dövrə lövhələrinin istehsalı texnologiyası hazır məhsuldan axın qalıqlarının məcburi çıxarılmasını təmin edir. Adətən, lehimləmə zamanı istifadə olunan rozin axını yalnız spirt-aseton qarışıqları ilə çıxarıla bilər, bu prosedurun yanğın təhlükəsi səbəbindən son dərəcə əlverişsizdir, bəzi KPYAK-lara əsaslanan axınlar isə su ilə yuyulur.
3. Kənd təsərrüfatı üçün antianemiya və antixloroz preparatları. Müəyyən edilmişdir ki, bir sıra 3d-keçid metallarının (Cu 2+ , Zn 2+ , Co 2+ və s.) CPAC ilə ionlarının kompleksləri yüksək bioloji aktivliyə malikdir. Bu, onların əsasında xəzçilikdə xəz heyvanların (ilk növbədə mink) alimentar anemiyasının qarşısının alınması və müalicəsi üçün effektiv antianemiya dərmanları və yetişdirilən meyvə və giləmeyvə bitkilərinin (xüsusilə üzüm) xlorozunun qarşısının alınması və müalicəsi üçün antixloroz dərmanları yaratmağa imkan verdi. karbonatlı torpaqlarda (ölkənin cənub rayonları). ) və bu səbəbdən xloroza meyilli. Şərtlərdə tam məhv olmaq qabiliyyətinə görə də qeyd etmək vacibdir mühit, KPJAK ekoloji cəhətdən təmiz məhsullardır.
Yuxarıda göstərilən sahələrə əlavə olaraq, CNC-də antikorroziya fəaliyyətinin olması, onlardan istifadənin mümkünlüyü göstərilmişdir. kimyəvi analiz, tibb və bəzi digər sahələr. KPYAK-ın alınması üsulları və onların praktik tətbiq müxtəlif sahələrdə bu hesabatın müəllifləri tərəfindən ixtiralar və patentlər üçün çoxsaylı müəllif hüquqları sertifikatları ilə qorunur.
Biblioqrafik keçid
Nikolsky V.M., Pchelkin P.E., Sharov S.V., Knyazeva N.E., Gorelov I.P. SƏNAYƏ VƏ KƏND TƏSƏRRÜFATINDA KOMPLEKSONLARIN, SANKİN TURŞUSUNUN TƏRƏMƏLƏRİNİN SİNTEZİ VƏ TƏTBİQİ // Müasir təbiət elminin uğurları. - 2004. - No 2. - S. 71-71;URL: http://natural-sciences.ru/ru/article/view?id=12285 (giriş tarixi: 01/05/2020). “Akademiya Təbiət Tarixi” nəşriyyatında çap olunan jurnalları diqqətinizə çatdırırıq.
Sinif üçün dikarboksilik turşular tərkibində iki karboksil qrupu olan birləşmələr daxildir. Dikarboksilik turşular karbohidrogen radikalının növündən asılı olaraq aşağıdakılara bölünür:
doymuş;
doymamış;
aromatik.
Dikarbon turşularının nomenklaturası monokarboksilik turşuların nomenklaturasına oxşar (2-ci hissə, 6.2-ci fəsil):
əhəmiyyətsiz;
radikal funksional;
sistematik.
Dikarboksilik turşuların adlarına dair nümunələr cədvəl 25-də verilmişdir.
Cədvəl 25 - Dikarbon turşularının nomenklaturası
|
Struktur formul |
ad |
||
|
əhəmiyyətsiz |
sistematik |
radikal funksional |
|
|
oksalat turşusu |
etandioik turşu | ||
|
|
malon turşusu |
propanedioik turşu |
metandikarboksilik turşu |
|
|
kəhrəba turşu |
butan turşu |
etandikarboksilik-1,2 turşusu |
|
|
qlutar turşusu |
pentandium turşu |
propandikarboksilik-1,3 turşusu |
|
|
adipik turşu |
heksanium turşu |
butandikarboksilik-1,4 turşusu |
|
|
malein turşusu |
cis-butendioic turşusu |
cis-etilendikarboksilik-1,2 turşusu |
|
Cədvəl 25 davam etdi |
|||
|
|
fumar turşusu |
trans-butenedioik turşu |
trans-etilendikarboksilik-1,2 turşusu |
|
|
itacon turşusu |
propen-2-dikarboksilik-1,2 turşusu |
|
|
butindioik turşu |
asetilendikarboksilik turşu |
||
|
|
ftal turşusu |
1,2-benzendikarboksilik turşu |
|
|
|
izoftalik turşu |
1,3-benzendikarboksilik turşu |
|
|
|
tereftalik turşu |
1,4-benzendikarboksilik turşu |
|
İzomerizm. Dikarboksilik turşular aşağıdakı izomerizm növləri ilə xarakterizə olunur:
Struktur:
skelet.
Məkan :
optik.
Dikarbon turşularının alınması üsulları. Dikarboksilik turşular monokarboksilik turşularla eyni üsullarla əldə edilir, ayrı-ayrı turşulara tətbiq olunan bir neçə xüsusi üsul istisna olmaqla.
Dikarbon turşularının alınmasının ümumi üsulları
Diolların və siklik ketonların oksidləşməsi:

Nitrillərin hidrolizi:

Diol karbonilləşməsi:
Oksalik turşunun alınması bərk qələvi varlığında əridərək natrium formatdan:
Malon turşusunun alınması:
Adipik turşunun alınması. Sənayedə mis-vanadium katalizatorunun iştirakı ilə sikloheksanolun 50% azot turşusu ilə oksidləşməsi yolu ilə əldə edilir:

Dikarbon turşularının fiziki xassələri. Dikarboksilik turşular bərk maddələrdir. Seriyanın aşağı üzvləri suda yüksək dərəcədə həll olunur və üzvi həlledicilərdə çox az həll olunur. Suda həll olunaraq molekullararası hidrogen bağları əmələ gətirirlər. Suda həllolma həddi buradadır FROM 6 - FROM 7 . Bu xüsusiyyətlər olduqca təbii görünür, çünki qütb karboksil qrupu molekulların hər birinin əhəmiyyətli bir hissəsidir.
Cədvəl 26 - Dikarbon turşularının fiziki xassələri
|
ad |
Düstur |
Belə ki, pl. °C |
20 °C-də həllolma, q/100 q |
10 5 × K 1 |
10 5 × K 2 |
|
turşəng | |||||
|
Malonik |
| ||||
|
Ənbər |
| ||||
|
Qlutarik |
| ||||
|
Adipin |
| ||||
|
boru kəməri |
| ||||
|
Mantar (suberik) |
| ||||
|
Azelaik |
| ||||
|
Sebacine |
| ||||
|
Maleic |
| ||||
|
Fumarovaya |
| ||||
|
Ftal |
|
Cədvəl 27 - Dikarbon turşularının qızdırıldığı zaman davranışı
|
Turşu |
Düstur |
Tbalya, °С |
reaksiya məhsulları |
|
turşəng |
CO 2 + HCOOH |
||
|
Malonik |
|
CO 2 + CH 3 COOH |
|
|
Ənbər |
|
|
|
|
Cədvəl 27 davam edir |
|||
|
Qlutarik |
|
|
|
|
Adipin |
|
|
|
|
boru kəməri |
|
|
|
|
Ftal |
|
|
|
Alkoqolların və xloridlərin ərimə və qaynama nöqtələri ilə müqayisədə turşuların yüksək ərimə nöqtələri, görünür, hidrogen bağlarının gücü ilə əlaqədardır. Qızdırıldıqda dikarbon turşuları müxtəlif məhsullar əmələ gətirmək üçün parçalanır.
Kimyəvi xassələri.İki əsaslı turşular karboksilik turşulara xas olan bütün xüsusiyyətləri saxlayır. Dikarboksilik turşular duzlara çevrilir və monokarboksilik turşular (turşu halogenidləri, anhidridlər, amidlər, efirlər) ilə eyni törəmələri əmələ gətirir, lakin reaksiyalar ya birində (natamam törəmələrdə) və ya hər iki karboksil qrupunda gedə bilər. Törəmə reaksiyalarının mexanizmi monokarboksilik turşuların mexanizmi ilə eynidir.
İki əsaslı turşular da ikisinin təsiri ilə bir sıra xüsusiyyətlər göstərir UNSD-qruplar.
turşu xüsusiyyətləri. Dikarbon turşuları doymuş bir əsaslı turşularla müqayisədə artan turşu xassələrinə malikdir (orta ionlaşma sabitləri, cədvəl 26). Bunun səbəbi təkcə ikinci karboksil qrupunda əlavə dissosiasiya deyil, çünki ikinci karboksilin ionlaşması daha çətin olur və ikinci sabitin turşu xassələrinə töhfəsi demək olar ki, nəzərə çarpmır.
Elektron çəkən qrup, məlum olduğu kimi, karboksilik turşuların turşu xüsusiyyətlərinin artmasına səbəb olur, çünki karboksil karbon atomunda müsbət yükün artması mezomer effektini artırır. р,π-konjugasiya, bu da öz növbəsində bağın qütbləşməsini gücləndirir ODUR və onun dissosiasiyasını asanlaşdırır. Bu təsir daha qabarıqdır, karboksil qrupları bir-birinə nə qədər yaxındırsa. Oksalik turşunun toksikliyi ilk növbədə onun yüksək turşuluğu ilə bağlıdır, dəyəri mineral turşularınkinə yaxınlaşır. Təsirin induktiv xarakterini nəzərə alsaq, aydın olur ki, dikarbon turşularının homoloji sıralarında turşu xassələri kəskin şəkildə azalır. karboksil qrupları bir birindən.
Dikarbon turşuları iki əsaslı turşular kimi davranır və iki sıra duz əmələ gətirir - turşu (bir əsas ekvivalenti ilə) və orta (iki ekvivalenti ilə):
Nukleofil əvəzetmə reaksiyaları . Dikarboksilik turşular, monokarboksilik turşular kimi, bir və ya iki funksional qrupun iştirak etdiyi nukleofil əvəzetmə reaksiyalarına daxil olur və funksional törəmələr - efirlər, amidlər, turşu xloridləri əmələ gətirir.

Okzalik turşunun özünün yüksək turşuluğuna görə onun efirləri turşu katalizatorlarından istifadə etmədən alınır.
3. Dikarbon turşularının spesifik reaksiyaları. Dikarboksilik turşularda karboksil qruplarının qarşılıqlı düzülüşü onların kimyəvi xassələrinə əhəmiyyətli dərəcədə təsir göstərir. İlk homoloqlar olan UNSD-qruplar yaxındır, - oksalik və malon turşuları - qızdırıldıqda karbonmonoksiti (IV) ayıra bilir, nəticədə karboksil qrupu çıxarılır. Dekarboksilləşmə qabiliyyəti turşunun quruluşundan asılıdır. Monokarboksilik turşular yalnız duzları bərk qələvilərlə qızdırıldıqda karboksil qrupunu daha çətin itirirlər. Turşu molekullarına daxil olduqda EAəvəzedicilər, onların dekarboksilləşmə meyli artır. Oksalik və malon turşularında ikinci karboksil qrupu belə fəaliyyət göstərir EA və bununla da dekarboksilləşməni asanlaşdırır.
3.1

3.2

Qarışqa turşusunun sintezi üçün laboratoriya üsulu kimi oksalat turşusunun dekarboksilləşməsindən istifadə olunur. Malon turşusu törəmələrinin dekarboksilləşməsi karboksilik turşuların sintezində mühüm mərhələdir. Di- və trikarboksilik turşuların dekarboksilləşməsi bir çox biokimyəvi proseslər üçün xarakterikdir.
Karbon zənciri uzandıqca və funksional qruplar çıxarıldıqca, onların qarşılıqlı təsiri zəifləyir. Odur ki, homoloji silsilənin növbəti iki üzvü - suksinik və qlutar turşuları qızdırıldıqda dekarboksilləşmir, lakin su molekulunu itirərək siklik anhidridlər əmələ gətirir. Reaksiyanın bu gedişi sabit beş və ya altı üzvlü dövrənin formalaşması ilə əlaqədardır.
3.3

3.4 Bir turşunun birbaşa esterifikasiyası ilə onun tam efirlərini, anhidridin ekvimolyar miqdarda spirt ilə qarşılıqlı təsirindən müvafiq turşu efirlərini əldə etmək olar:
3.4.1

3.4.2

3.5 İmidlərin hazırlanması . Süksinik turşunun ammonium duzunu qızdırmaqla onun imidi (süksinimid) alınır. Bu reaksiyanın mexanizmi monokarboksilik turşuların duzlarından amidlərin hazırlanmasında olduğu kimidir:
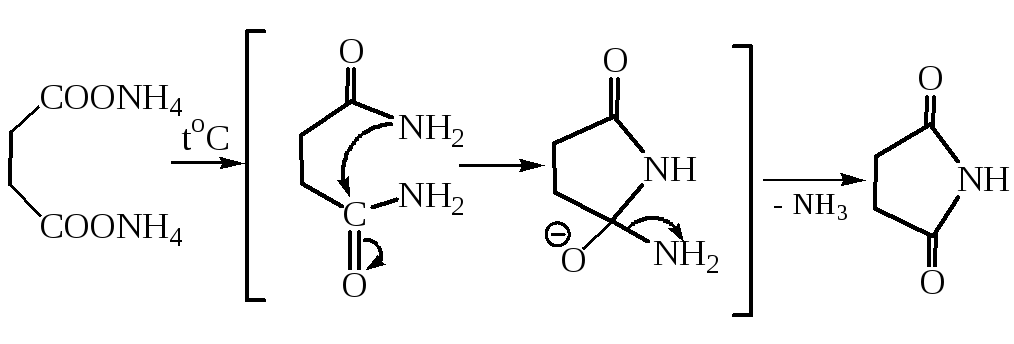
Süksinimiddə, imino qrupundakı hidrogen atomu əhəmiyyətli bir proton hərəkətliliyinə malikdir, bu, iki qonşu karbonil qrupunun elektron çəkmə təsirindən qaynaqlanır. Bu, əldə etməyə əsaslanır N-bromo-süksinimid - bromun allil mövqeyinə daxil edilməsi üçün bromlaşdırıcı agent kimi geniş istifadə olunan birləşmə:

fərdi nümayəndələr. Oksalik (etandik) turşu IEP– UNSD. Turşəng, turşəng, rhubarb yarpaqlarında olan duzlar şəklində. Oksalat turşusunun duzları və efirləri oksalatların mənasız adına malikdir. Oksalat turşusu azaldıcı xüsusiyyətlərə malikdir:
Bu reaksiya kalium permanqanat məhlullarının dəqiq konsentrasiyasını təyin etmək üçün analitik kimyada istifadə olunur. Kükürd turşusunun iştirakı ilə qızdırıldıqda, oksalat turşusunun dekarboksilləşməsi baş verir, sonra əmələ gələn qarışqa turşusunun parçalanması baş verir:
Oksalik turşunun və onun duzlarının aşkarlanması üçün keyfiyyətli reaksiya həll olunmayan kalsium oksalatın əmələ gəlməsidir.
Oksalat turşusu asanlıqla oksidləşir, kəmiyyətcə karbon qazına və suya çevrilir:
Reaksiya o qədər həssasdır ki, kalium permanqanat məhlullarının titrlərini təyin etmək üçün həcm analizində istifadə olunur.
Malon turşusu (propandioik). IEP– CH 2 – UNSD. Şəkər çuğunduru şirəsində var. Malon turşusu, iki karboksil qrupunun elektron çəkmə təsirinə görə metilen qrupundakı hidrogen atomlarının əhəmiyyətli proton hərəkətliliyi ilə fərqlənir.
Metilen qrupunun hidrogen atomları o qədər hərəkətlidir ki, onları metal ilə əvəz etmək olar. Bununla birlikdə, sərbəst bir turşu ilə bu çevrilmə mümkün deyil, çünki karboksil qruplarının hidrogen atomları daha çox hərəkətlidir və əvvəlcə əvəz olunur.
Əvəz edin α -metilen qrupunun hidrogen atomlarının natriuma çevrilməsi yalnız karboksil qruplarını qarşılıqlı təsirdən qorumaqla mümkündür ki, bu da malon turşusunun tam esterləşməsinə imkan verir:

Malonik ester, natrium ilə qarşılıqlı əlaqədə olduqda, hidrogeni parçalayaraq, natrium-malonik ester əmələ gətirir:

Anion Na- konjugasiya ilə sabitləşən malonik ester NEP karbon atomu ilə π - bağ elektronları C=HAQQINDA. Na-malonik ester, bir nukleofil olaraq, elektrofilik mərkəzi olan molekullarla, məsələn, haloalkanlarla asanlıqla reaksiya verir:
Sadalanan reaksiyalar bir sıra birləşmələrin sintezi üçün malon turşusundan istifadə etməyə imkan verir:

süksin turşusu ilə rəngsiz kristal maddədir. 183 °C, suda və spirtdə həll olunur. Süksinik turşu və onun törəmələri olduqca əlçatandır və üzvi sintezdə geniş istifadə olunur.
Adipik (heksandioik) turşusu HOOS-(CH 2 ) 4 -COOH. Rəngsiz kristal maddəni belə pl ilə təmsil edir. 149 ° C, suda bir az həll olunur, daha yaxşı - spirtlərdə. Poliamid neylon lifi hazırlamaq üçün çox miqdarda adipin turşusu istifadə olunur. Turşu xüsusiyyətlərinə görə, adipin turşusu gündəlik həyatda emaye qablardan kirəyi çıxarmaq üçün istifadə olunur. Kalsium və maqnezium karbonatları ilə reaksiya verir, onları həll olunan duzlara çevirir və eyni zamanda güclü mineral turşular kimi minaya zərər vermir.































